La prevenzione oncologica in ginecologia
Grandi scoperte della Medicina sono state spesso il frutto di osservazioni apparentemente banali coniugate alle intuizioni di chi sa vedere perché vuole vedere. Penso alla più travagliata e tragica storia di Ignaz Philip Semmelweis, l’ostetrico ungherese che nell’Ottocento intuì l’origine infettiva della febbre puerperale, opponendosi al pensiero scientifico dell’epoca, che non era né “pensiero” né “scientifico”, bensì solo ideologia. La storia, il tempo, rende ragione alla verità, almeno a quella scientifica, e Papanicolau è stato più fortunato di Semmelweis perché la sorte gli ha permesso di vedere il frutto della sua intuizione.
Il Pap-test obbedisce a tutti i criteri delineati da Sackett per poterlo offrire alla popolazione femminile come screening (raccomandazione n° 9 del Codice Europeo Contro il Cancro): il cancro del collo dell’utero è potenzialmente piuttosto frequente ed associato a rilevante morbilità. Ne è ormai nota la storia naturale (cioè si conoscono le modalità con cui evolve): lesioni precancerose precedono lo sviluppo del tumore propriamente detto. Il test permette di identificarle ed alla diagnosi segue un trattamento che, benché comunque chirurgico, è locale, limitato, non priva la donna dell’utero e della sua funzione, e conduce alla guarigione definitiva nella quasi totalità dei casi; ha pochi “falsi negativi” e pochi “falsi positivi”, è rapido, di semplice esecuzione, atraumatico e di basso costo.
I motivi del successo del Pap-test sono fin troppo ovvi: da una parte la progressione che porta dalla lesione pretumorale al cancro è un processo molto lento, dall’altra il collo dell’utero è facilmente accessibile e disponibile a prelievi diretti (è sufficiente introdurre uno speculum nella vagina per poterlo vedere, ed il tumore nasce proprio, nella maggior parte dei casi, da zone visibili). Il successo, allora, non ci stupisce più di tanto: potrebb’essere ipotizzabile un prelievo diretto dallo stomaco, dall’intestino, dalla prostata, dalla mammella, dalle ovaie od anche solo dall’interno dell’utero? La risposta è ovvia: no. E quindi per gli altri organi s’impongono strategie diverse, che non sono più prevenzione ma, al massimo e quando è possibile, diagnosi precoce.
Se ogni donna si sottoponesse periodicamente al test di Papanicolau potremmo teoricamente veder azzerare l’incidenza del cancro del collo dell’utero. Per ciò che attiene alla periodicità, l’esperienza personale mi suggerisce che la ripetizione del Pap-test ogni 2-3 anni sia quella da ritenersi ottimale: non ho mai identificato una lesione tale da richiedere l’ablazione dell’apparato genitale se non in donne che non si sottoponevano al Pap-test da più di 3-5 anni. Almeno finora.
Un’altra pietra miliare nella comprensione della storia naturale del cancro del collo dell’utero l’ha posta un italiano, Domenico Rigoni Stern. Studiando i registri mortuari della provincia di Ve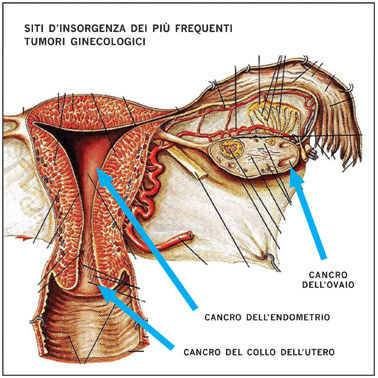 rona, aveva notato che le donne che morivano per questa malattia erano sposate, mentre non si riscontrava mortalità tra le nubili. Quest’osservazione gli permise di ipotizzare, già nel 1842, che un qualche fattore sessualmente trasmesso potesse intervenire nella genesi di questo tumore. Le ricerche degli anni seguenti focalizzarono l’attenzione su vari agenti infettivi; e dal 1983 si crede che la cancerogenesi del collo dell’utero sia avviata da un virus – l’HPV (Human Papilloma Virus).
rona, aveva notato che le donne che morivano per questa malattia erano sposate, mentre non si riscontrava mortalità tra le nubili. Quest’osservazione gli permise di ipotizzare, già nel 1842, che un qualche fattore sessualmente trasmesso potesse intervenire nella genesi di questo tumore. Le ricerche degli anni seguenti focalizzarono l’attenzione su vari agenti infettivi; e dal 1983 si crede che la cancerogenesi del collo dell’utero sia avviata da un virus – l’HPV (Human Papilloma Virus).
Recentemente è stato messo a punto un esame, l’HPV-test, volto ad identificare la presenza di questo virus nella via genitale femminile, con lo scopo di selezionare quelle donne che, portatrici anche sane, sono da ritenersi più a rischio e quindi vanno sorvegliate con maggiore frequenza, mentre le non-portatrici sono da ritenersi prive di rischio, almeno sulla breve scadenza (5 anni). La proposta di associare l’HPV-test al Pap-test nello screening del cancro del collo dell’utero si fonda su alcuni dati importanti della letteratura internazionale, ed inquietanti (tra cui quello della francese Clevel), secondo i quali il test di Papanicolau risulterebbe falsamente negativo nel 30-50% dei casi. L’errore è umanamente e tecnicamente sempre possibile, e questa possibilità va tenuta presente, ma l’esperienza personale non mi consente di confermare quest’allarme. Ritengo pertanto che il test virale abbia attualmente il suo miglior impiego nelle donne con Pap-test dubbio, casi in cui si deve scegliere tra un comportamento solo osservazionale oppure attivo.
Il futuro? Credo che l’HPV-test sostituirà il Pap-test nello screening del cancro del collo dell’utero: i presupposti culturali sono convincenti, ma non è ancora giunto il momento per proporre alle donne un HPV-test ogni 5 anni al posto di un Pap-test ogni 2-3. L’identificazione di un virus quale agente causale di questo tumore sta consentendo la messa a punto di un vaccino specifico, ma i risultati e le modalità di applicazione non sono ancora trasferibili dal campo della ricerca a quello della pratica applicazione clinica. Disponiamo, dunque, di uno strumento molto efficace, il Pap-test, per la lotta ad un tumore che, però, è divenuto alquanto raro; e disporremo di un’altra arma – il vaccino – per un tumore comunque già dominato. Magari avessimo a disposizione simili strumenti per i tumori che, per frequenza, preoccupano di più, come il cancro della mammella o quello dell’ovaio.
Attualmente è il cancro dell’endometrio il più frequente tumore maligno dell’apparato genitale femminile. Insorge dalla cavità uterina, appunto dall’endometrio, cioè dalla mucosa che la riveste dall’interno. Non esiste alcuna forma di prevenzione simile al Pap-test e la lotta contro questo tumore si fonda sulla diagnosi precoce, all’occorrenza del primo sintomo: il sanguinamento genitale anormale (raccomandazione n° 8 del Codice Europeo Contro il Cancro), con ciò intendendo quello che si verifica al di fuori del normale ciclo mestruale e, soprattutto, in menopausa, dal momento che questo tumore è pressoché assente prima dei 40 anni e l’assoluta maggioranza dei casi si realizza dopo la cessazione definitiva delle mestruazioni.
Nell’esperienza personale solo il 10% dei sanguinamenti genitali anormali è sintomo di un cancro dell’endometrio in evoluzione, mentre negli altri casi o non c’è patologia affatto o, al massimo, esiste una patologia benigna; ma, all’occorrenza di questo sintomo, faranno seguito indagini non invasive, come l’ecografia, e, se indicato, indagini più invasive come l’isteroscopia (esame endoscopico, quindi visivo, della cavità uterina) e la biopsia dell’endometrio. Così facendo, la maggioranza dei cancri dell’endometrio viene identificata comunque al primo stadio di malattia e la chirurgia che segue conduce alla guarigione definitiva nell’assoluta maggioranza dei casi, anche perché questo tumore, se pure è diventato il più frequente, è anche fortunatamente il meno aggressivo tra quelli ginecologici. Sottoponendo tutta la popolazione femminile in menopausa periodicamente ad un’ecografia di screening, si giungerebbe solo occasionalmente a diagnosi più precoci di quelle ottenute attendendo la comparsa del primo sintomo, ed inoltre non si otterrebbe una significativa diminuzione della mortalità per un tumore che registra percentuali di guarigione comunque molto alte, anche se per porre la diagnosi si attende la comparsa del primo sintomo. Non si ritiene, pertanto, che l’ecografia, benché innocua, indolore e priva di rischio, sia un esame da proporre come screening del cancro dell’endometrio.
Ma la grande sfida per il ginecologo è attualmente rappresentata dal cancro dell’ovaio, secondo per frequenza tra i tumori dell’apparato genitale femminile, ma il più preoccupante perché – è triste ma doveroso ammetterlo – non esiste alcuna forma di diagnosi precoce ed ancora viene identificato al terzo stadio di malattia nel 75% dei casi. E questo, sia chiarissimo, non è dovuto ad incapacità o disattenzione bensì a precise motivazioni che riguardano l’anatomia dell’addome e la storia naturale di questo tumore.
Famoso, e dalle conclusioni insuperate, è lo studio del 1990 di Stuart Campbell, ginecologo inglese, uno dei padri dell’ecografia (Campbell S. – “Novel screening strategies for early ovarian cancer by transabdominal ultrasonography” – British Journal of Obstetrics and Gynaecology, 97: 304-311, 1990): egli sottopose ad ecografia 5479 donne asintomatiche, con lo scopo di giungere alla diagnosi precoce del cancro dell’ovaio, eseguendo tre ecografie all’anno su ciascuna di esse; 326 donne risultarono sospette per la presenza di un carcinoma ovarico e tutte vennero sottoposte a chirurgia; i carcinomi realmente identificati furono soltanto cinque. Queste gli avranno sicuramente eretto un monumento, ma le altre 321?
L’esperienza di Campbell non è stata sostanzialmente smentita nemmeno dall’avvento dell’ecografia transvaginale, e la conclusione è evidente: l’ecografia non può essere impiegata come mezzo di screening del cancro dell’ovaio; il costo pagato in termini di inutile chirurgia sarebbe troppo alto. Tradizionalmente l’invito alle donne di sottoporsi annualmente al controllo ginecologico avrebbe come scopo principale quello di identificare precocemente un cancro dell’ovaio in evoluzione ma ancora asintomatico: questo impariamo dai testi sacri della ginecologia, e questo sanno le donne. L’esperienza personale non mi permette di credere ancora, dopo vent’anni, che questa sia una misura preventiva efficace per anticipare la diagnosi e migliorare le possibilità di cura e la prognosi: solo una volta, infatti, ho identificato un cancro dell’ovaio di piccole dimensioni ed ancora completamente asintomatico nell’occasione di una visita ginecologica “di controllo”; ed anche in quel caso il tumore era già al terzo stadio, il che praticamente significa chirurgia seguita da chemioterapia. La diagnosi sarà pure stata brillante, ma non certo precoce. I colleghi a cui ho chiesto “a te quante volte è capitato?” mi hanno risposto in maniera aneddotica, confermando sostanzialmente quella che fin qui è la mia esperienza diretta.
Non ci credo più e, soprattutto, non mi sento più di promettere alle donne quello che so di non poter mantenere: la “visita ginecologica di controllo” come momento di diagnosi precoce del cancro dell’ovaio. Condivido, quindi, l’impostazione che gli esperti hanno dato al Codice Europeo Contro il Cancro, nel quale la visita ginecologica periodica non viene suggerita. E nemmeno l’ormai noto marcatore ematico CA-125, indispensabile nel controllo postchirurgico e postchemioterapico delle donne trattate per cancro dell’ovaio, può essere utilizzato a scopo di screening: in circa il 20% dei casi il marcatore è comunque negativo, ed inoltre è un indicatore troppo aspecifico e numerose altre condizioni, anche non patologiche, possono determinarne l’elevazione e porterebbero ad indagini invasive, anche chirurgiche, che poi si dimostrerebbero infondate nella maggior parte dei casi; e questo senza voler parlare dell’ansia indotta da un risultato anormale.
Attualmente si ritiene che le uniche misure realmente efficaci nella prevenzione del cancro dell’ovaio siano da una parte l’asportazione delle ovaie nelle donne prossime alla menopausa o in menopausa cui viene asportato l’utero per una patologia benigna, e, dall’altra, il controllo periodico (visita, ecografia e determinazione del CA-125) delle donne con una predisposizione familiare per questa malattia oncologica. Ma solo il 5% dei cancri dell’ovaio riconosce un’origine familiare; e, nell’eventualità che tale predisposizione sia particolarmente preoccupante, si dovrebbe prendere in considerazione l’idea dell’asportazione profilattica delle ovaie anche in assenza di patologia. Se, una volta completato il programma riproduttivo, è accettata l’idea della sterilizzazione chirurgica perché non può esserlo quella dell’asportazione delle ovaie in donne con rischio familiare specifico elevato?
Quello che mi stupisce abbastanza è come sia poco considerato il dato della letteratura, ormai indiscusso, che conferma come l’impiego protratto della “pillola” riduca significativamente (forse più del 50%) il rischio di sviluppare un cancro dell’ovaio (“Neoplasie dell’ovaio”, in: Società Italiana di Oncologia Ginecologica – “Manuale di Ginecologia Oncologica” – UTET, Torino 1998), e, probabilmente, anche quello dell’endometrio: questo mi pare un beneficio extracontraccettivo di grande rilevanza che fa della “pillola” un farmaco veramente prezioso. Non ne esiste altro che abbia una simile potenza preventiva. Chissà perché, ma della “pillola” vengono spesso enfatizzati i possibili e rarissimi rischi, come quello tromboembolico, mentre vengono minimizzati i benefici che può avere anche in donne sessualmente inattive.
L’esperienza personale mi permette, oggi, di credere che solo quelle che di seguito riassumo siano le misure che hanno una realistica potenza nel ridurre la morbilità o la mortalità per tumore ginecologico:
1) Sottoporsi al Pap-test ogni 2-3 anni.
2) Sottoporsi ad esame ginecologico ed ecografia transvaginale in caso di sanguinamento genitale anormale, soprattutto dopo i 40 anni e soprattutto se tale sanguinamento si verifica in menopausa.
3) Nel corso di un intervento chirurgico ginecologico eseguito per altra patologia asportare le ovaie: se la donna è già in menopausa; se la donna ha una familiarità per cancro dell’ovaio ed ha completato il suo programma riproduttivo. Offrire la stessa possibilità alle donne non ancora in menopausa ma, per età, statisticamente prossime ad essa.
4) Per le donne con familiarità per cancro dell’ovaio: esame ginecologico, ecografia e determinazione del CA-125 ogni 6-12 mesi o, eventualmente, asportazione profilattica delle ovaie se il programma riproduttivo è stato completato e se il rischio familiare è significativo o tale da generare un’ansia eccessiva.
5) Preferire il contraccettivo orale agli altri mezzi di prevenzione del concepimento, quando possibile ed in assenza di controindicazioni specifiche.
Il resto è fantasia o fede nel futuro.
dott. Francesco Morosetti, ginecologo